A esclerose múltipla (EM) é amplamente conhecida como uma doença autoimune em que o corpo ataca a bainha protetora de mielina que envolve as fibras nervosas. No entanto, um estudo inovador publicado na Nature revela um mecanismo mais profundo e insidioso que conduz a fase mais debilitante da doença: a morte de células cerebrais específicas que sustentam a cognição humana.
Os investigadores identificaram porque é que certos neurónios são exclusivamente vulneráveis à EM, descobrindo uma falha biológica que pode explicar porque é que os tratamentos actuais não conseguem parar o declínio cognitivo e o encolhimento do cérebro em fases progressivas da doença.
O custo oculto de ser humano
O estudo se concentra em um grupo específico de neurônios conhecidos como células CUX2, localizados na camada mais externa do córtex cerebral. Estas células são essenciais para funções cognitivas complexas, como o raciocínio e o processamento da memória – características que distinguem a inteligência humana da de outros mamíferos.
Embora essas células sejam essenciais para o pensamento de alto nível, elas apresentam uma compensação biológica. Durante o desenvolvimento inicial do cérebro, os neurônios CUX2 se multiplicam a uma taxa excepcionalmente rápida. Essa velocidade, no entanto, aumenta a probabilidade de danos ao DNA se acumularem dentro das células.
Para sobreviver a esse estresse de desenvolvimento, essas células dependem de um “kit de reparo” especializado, impulsionado por uma proteína chamada ATF4. Esta proteína inicia a resposta de reparação do ADN, evitando danos catastróficos à medida que os neurónios amadurecem. Sem ATF4, estas células não conseguem suportar o seu rápido crescimento e morrem.
Quando o mecanismo de reparo falha
A descoberta crítica reside no que acontece quando estas células já estressadas encontram a inflamação da esclerose múltipla.
Em cérebros saudáveis, o sistema de reparação mediado pelo ATF4 mantém os danos no ADN sob controlo. Contudo, em pacientes com EM, a inflamação crónica sobrecarrega este sistema. Os pesquisadores descobriram que:
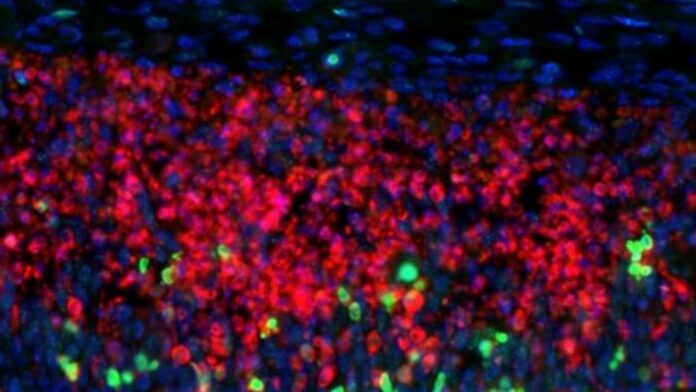
* Maiores danos ao DNA: O tecido cerebral de pacientes com esclerose múltipla mostrou níveis significativamente elevados de danos ao DNA nas camadas onde residem os neurônios CUX2, em comparação com cérebros saudáveis.
* Colapso Celular: Em camundongos projetados para imitar condições de EM, as células CUX2 morreram especificamente devido a esse dano acumulado no DNA.
* Limiar de Vulnerabilidade: A inflamação causada pela EM empurra essas células além do seu ponto de ruptura. Como já estão sobrecarregados com os riscos do seu rápido desenvolvimento inicial, falta-lhes a resiliência necessária para lidar com o stress adicional de um ataque autoimune.
“Vemos esse tipo de tema consistente de que essas células simplesmente não lidam muito bem com esse estresse extra”, diz David Rowitch, neurocientista do desenvolvimento da Universidade de Cambridge e coautor do estudo.
Um novo alvo para tratamento
Esta descoberta desafia o foco tradicional da investigação da EM. Durante décadas, as terapias tiveram como objetivo principal restaurar a mielina ou suprimir o sistema imunológico para reduzir a inflamação. Embora estas abordagens ajudem a gerir sintomas e crises, não abordam a vulnerabilidade celular subjacente que leva à atrofia cerebral progressiva.
“A descoberta aponta para um novo local para direcionar tratamentos futuros”, observa Rowitch. Atualmente, não existe um tratamento eficaz para a fase progressiva da EM, onde os neurônios morrem e os pacientes apresentam declínios acentuados na memória e no raciocínio.
Don Mahad, neurologista da Universidade de Edimburgo que não esteve envolvido na investigação, enfatiza a mudança de perspectiva que este estudo exige. “Isso nos diz que, na verdade, não podemos ignorar essas vulnerabilidades intrínsecas das células nervosas, e isso tem que ser um alvo de tratamento”, diz ele.
Conclusão
A identificação da vulnerabilidade dos neurônios CUX2 oferece um elo perdido crucial na compreensão da esclerose múltipla progressiva. Ao reconhecer que a capacidade de reparação do ADN é tão crítica como a supressão imunitária, os cientistas podem agora explorar terapias concebidas para proteger estas células frágeis de danos internos, potencialmente travando o declínio cognitivo que atualmente define as fases posteriores da doença.